Facebook для біотеху. Як ШІ-проєкт Цукерберга планує лікувати людство
- Єлизавета Гогілашвілі

- 22 години тому
- Читати 4 хв

Biohub, проєкт CEO Meta Марка Цукерберга та його дружини, педіатрині Прісцилли Чан, інвестував $500 млн у розробку ШІ-моделей людських клітин. Мета — «пришвидшити лікування та профілактику захворювань» за допомогою цифрових копій живих систем.
HBJ разом з експертами розповідає, що це означає для розвитку біотехнологій і як людство просунулось у лікуванні хвороб за останні роки.
Що таке Biohub
Chan Zuckerberg Biohub був заснований у 2016 році як некомерційна організація. Його глобальна місія звучить фантастично: «допомогти вилікувати, передбачити або контролювати всі хвороби до кінця століття».
З нещодавно проінвестованої половини мільярда $400 млн витратять на внутрішні дослідження самого Biohub, а $100 млн — на підтримку незалежних наукових груп. Важливою особливістю проєкту є принцип Open Science: всі розробки та зібрані дані будуть у відкритому доступі для світової наукової спільноти. На створення моделей прогнозують витратити пʼять років.

«Biohub — один із найамбітніших і водночас найбільш науково обґрунтованих проєктів у цьому напрямку. Їхня сильна сторона в тому, що вони поєднують ШІ-експертизу з реальною експериментальною біологією, а це критично важливо. У біотеху неможливо вирішити все лише алгоритмами без якісної роботи в лабораторії із біологічними зразками», — підкреслює докторка молекулярної біомедицини, наукова співробітниця Віра Єфремова.
Науковиця додає, що ідея створення базових моделей людських клітин — це логічний еволюційний крок для індустрії. Якщо такі моделі справді навчаться передбачати поведінку клітин у відповідь на зовнішні подразники (генетичні зміни, ліки, стрес тощо), це потенційно може змінити ранні етапи розробки терапій.
Особливо важливо, зазначає Віра, що проєкт Цукерберга та Чан робить ставку на одноклітинні та мультимодальні дані — саме вони дають найбільше інформації для розуміння поведінки клітин.

ШІ на ринку біотехнологій: від «жахіття» до прориву
Глобальний ринок ШІ в біотехнологіях оцінили у $3,27 млрд у 2024 році. Аналітики прогнозують, що у 2034 році він складатиме вже $18,76 млрд.
Крім проєкту Цукерберга і Чан, серед ключових рішень на цьому полі:
AlphaFold — ШІ-система від гуглівського DeepMind. Розробка прогнозує 3D-структури майже усіх відомих людству білків за їхніми амінокислотними послідовностями із точністю, що наближена до лабораторної.
До AlphaFold вчені вже знали послідовності, але не могли «згорнути» їх в 3D-структури. На передбачення структури тільки одного білка могли йти роки досліджень. Тепер це займає хвилини. Досягнення DeepMind прискорює створення ліків і розробку вакцин, а також допомагає вирощувати здоровіших бджіл чи термостійкі польові культури.
За свою розробку Деміс Хассабіс та Джон Джампер з DeepMind у 2024 році отримали Нобелівську премію з хімії.
Pharma.AI — платформа від компанії Insilico Medicine, яка спрощує розробку нових ліків. Rentosertib — перший препарат, у якому і мішень (білок, рецептор або молекулу, на яку націлений лікарський засіб — Ред.), і саму молекулу для таргетної терапії знайшли за допомогою генеративного ШІ на платформі Pharma.AI, — дійшов до останніх стадій клінічних досліджень.
DeepChem — open-source Python-бібліотека, яка надає інструменти для застосування глибинного навчання до хімічних і біологічних даних. Це потрібно зокрема при створенні нових ліків.
Раніше біотех-сектор вважався вкрай токсичним для венчурних інвесторів.

Як зазначає аналітик та підприємець Євген Найштетік, ще не так давно на розробку одного лікарського засобу йшло від 10 до 25 років.
Тому професійні біотех-інвестори розбивали фінансування на віхи: від пошуку молекули-кандидата до клінічних досліджень і виходу на ринок. Це був закритий клуб великих корпорацій, куди не могли собі дозволити зайти венчурні фонди. Якщо порівнювати з IT, на цьому ринку шалені ризики поєднувались із нескінченними термінами інвестування, що було абсолютно непривабливим.
Поступово парадигма змінилась і в медицині, і в способах створення ліків, і в інвестуванні — поява «органів на чипах» значно прискорила перші фази скринінгу і створення ліків, науковці відкрили нові хвороби і почали створювати таргетовану терапію.
Завдяки повній розшифровці геному і зниженню вартості генетичної діагностики став можливим збір великої кількості генетичних даних. Розвиток ШІ дозволив швидко й ефективно обробляти ці дані.
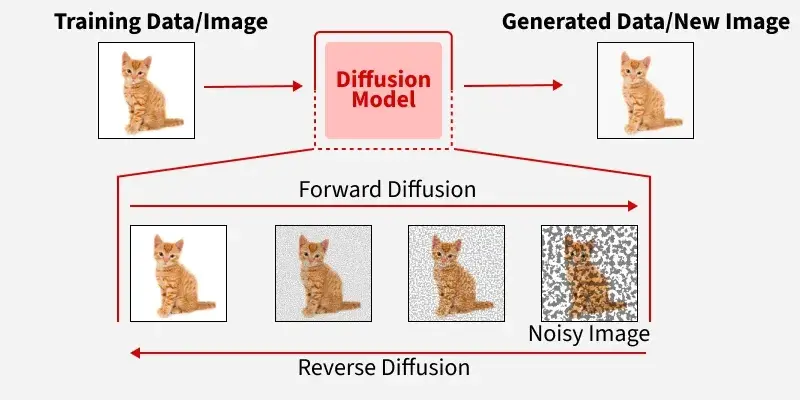
Після успіху генеративного ШІ у створенні контенту індустрія намагається перенести досвід у біологію. Лабораторія ШІ Google DeepMind використовує для досліджень структури протеїнів дифузійні моделі — ті самі, що генерують картинки в ChatGPT. Такі моделі спочатку «забруднюють» дані додатковим шумом, а потім поступово прибирають його, відновлюючи оригінальну інформацію.
Цукерберг і Чан в Biohub роблять ставку на структуру великих мовних моделей (LLM).
«Вони зрозуміли: якщо ДНК — це «мова життя», чому б не створити LLM для неї? Так з’явилася серія генеративних моделей для біології ESM (Evolutionary Scale Modeling), які започаткувала лабораторія Facebook AI. Такі моделі можна запустити на звичайному комп’ютері. Для клініки чи лабораторії це означає просту оркестрацію генетичних даних без хмарних сервісів», — говорить Євген.
Проте в роботі з біологічними даними є значний виклик — біологія набагато «шумніша» за текстові дані.
«У біології “шум” означає не просто технічні помилки, а природну варіабельність живих систем. Навіть клітини одного типу можуть сильно відрізнятися між собою залежно від віку, мікрооточення, рівня стресу, стадії клітинного циклу чи впливу запалення.
Крім того, результати можуть змінюватися через різні методи підготовки зразків, секвенування або лабораторні умови. Наприклад, під час одноклітинного аналізу РНК дві «однакові» клітини можуть демонструвати різні профілі експресії генів навіть у межах однієї
тканини. Через такі особливості біологічні дані складно стандартизувати», — пояснює Віра.
Яке майбутнє обіцяє Biohub
Віра Єфремова зазначає: біологія все ще набагато складніша, ніж більшість ШІ-систем здатні адекватно описати. Але алгоритми безперервно навчаються, тож відчутне посилення можливостей дослідників завдяки ШІ ще попереду. Одним з таких посилень може стати Biohub.
За п'ять років розвитку проєкту, каже нейробіологиня, цілком реально:
створити потужні базові моделі для конкретних типів тканин і клітин;
суттєво покращити прогнозування для досліджень та розробки ліків;
інтегрувати ШІ-моделі у фармацевтичні R&D-процеси.
Євген Найштетік впевнений — якщо все піде за планом, проєкт стане майданчиком для створення інновацій десятками тисяч команд. Biohub, як платформа, де можна відточувати діагностику і лікування, бачитиме, що створюють команди ще на ранніх етапах.
Це дозволить Цукербергу не просто розвивати науку, а й першим знаходити найбільш перспективні стартапи на ранніх етапах, прокладаючи шлях до фундаментального переформатування ринку охорони здоров'я.
Для звичайної людини успіх Biohub — це лише один із ймовірних сценаріїв, який обіцяє перехід від медицини «проб і помилок» до точної інженерії. У теорії, якщо цифрові моделі клітин доведуть свою ефективність, це може скоротити шлях нових ліків до аптеки з нинішніх 20 до 5–7 років.
Проте варто розуміти: біологія складніша за будь-який програмний код, і попереду ще безліч «невідомих» — від етичних питань використання ШІ до непередбачуваності живих систем, які не завжди підкоряються алгоритмам.
Якщо команді Цукерберга вдасться приборкати цей «біологічний шум», ми отримаємо шанс на персоналізовану терапію. Це дозволить не просто лікувати симптоми за загальними протоколами, а прогнозувати розвиток хвороби на цифровій копії конкретного пацієнта. Але чи стане цей амбітний проєкт реальністю, стане зрозуміло в найближчі п'ять років експериментів.




